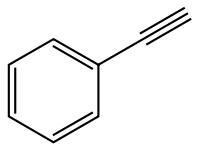
Фенилацетилен
| Фенилацетилен | |
 | |
 | |
| Общие | |
|---|---|
| Химическая формула | C8H6 |
| Физические свойства | |
| Молярная масса | 102.133 г/моль |
| Плотность | 0.93 г/см³ |
| Термические свойства | |
| Температура плавления | –45 °C |
| Температура кипения | 142-144 °C |
| Классификация | |
| Рег. номер CAS | 536-74-3 |
| SMILES | C#Cc1ccccc1 |
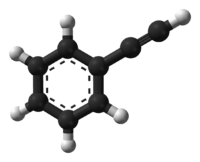
Фенилацетилен — углеводород, относящийся к классу алкинов и аренов.
Методы синтеза
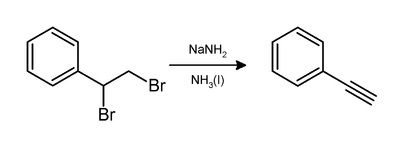
- Из 1,2-дибром-1-фенилэтана действием амида натрия в жидком аммиаке[1] :
Реакции
- Гидрирование до стирола или этилбензола.
- Тримеризация до 1,2,4(97 %) и 1,3,5 -трифенилбензолов [3]
Примечания
- ↑ Kenneth N. Campbell and Barbara K. Campbell (1963). «Phenylacetylene». Org. Synth.; Coll. Vol. 4: 763.
- ↑ John C. Hessler (1941). «Phenylacetylene». Org. Synth.; Coll. Vol. 1: 438.
- ↑ Gerhard Hilt , Thomas Vogler, Wilfried Hess, Fabrizio Galbiati (2005). «A simple cobalt catalyst system for the efficient and regioselective cyclotrimerisation of alkynes». Chemical Communications 2005 (11): 1474—1475. doi:10.1039/b417832g.
 |
 Углеводороды Углеводороды | |
|---|---|
| Алканы | Метан • Этан • Пропан • Бутан • Пентан • Гексан • Гептан • Октан • Нонан • Декан • Ундекан • Додекан • Тридекан • Тетрадекан • Гексадекан • Эйкозан . |
| Алкены | Этилен • Пропен • Бутен • Пентен • Гексен • Гептен • Октен . |
| Алкины | Ацетилен • Пропин • Бутин |
| Диены | Пропадиен • Бутадиен • Изопрен |
| Другие ненасыщеные | Винилацетилен • Диацетилен |
| Циклоалканы | Циклопропан • Циклобутан • Циклопентан • Циклогексан • Декалин • Индан |
| Ароматические | Бензол • Толуол • Диметилбензолы • Этилбензол • Пропилбензол • Кумол • Стирол • Фенилацетилен • Индан • Циклобутадиен • Дифенил • Дифенилметан • Трифенилметан • Тетрафенилметан |
| Полициклические | Нафталин • Антрацен • Пентацен • Фенантрен • Пирен • Бензпирен • Азулен • Хризен |
Wikimedia Foundation . 2010 .
Полезное
Смотреть что такое «Фенилацетилен» в других словарях:
фенилацетилен — фенилацетилен … Орфографический словарь-справочник
фенилацетилен — сущ., кол во синонимов: 1 • углеводород (77) Словарь синонимов ASIS. В.Н. Тришин. 2013 … Словарь синонимов
Фенилацетилен — см. Углеводороды ароматические … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
ФЕНИЛАЦЕТИЛЕН — (этинилбензол), мол. м. 102,14; бесцв. жидкость; т. пл. 44,8 0C, т. кип. 141,7 0C, 44 °С/18 мм рт. ст.; … Химическая энциклопедия
фенилацетилен — фенилацетиле/н, а … Слитно. Раздельно. Через дефис.
Фенилжирные кислоты — Эти ароматические соединения могут быть рассматриваемы как гомологи бензойной кислоты С6Н5 CO2Н, а с другой, как жирные кислоты, в которых один или несколько атомов водорода углеводородного радикала замещены фенилом (СбН5). По своим химическим… … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
Углеводороды ароматические — получили свое название оттого, что очень часто их производные обладают приятным запахом и встречаются в различных смолах, эфирных маслах и пр. Главным продуктом для их получения служит каменноугольная смола, образующаяся в довольно значительном… … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
КОНДАКОВА РЕАКЦИЯ — присоединение галогенангидридов карбоновых к т к олефинам и ацетиленам с образованием соотв. (b галогенкетонов и b галогенвинилкетонов: Катализаторами р ции, как правило, служат к ты Льюиса. Обычно для проведения К. р. готовят комплекс галогенан… … Химическая энциклопедия
МОЛИБДЕНОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ — содержат связь МоЧС. Помимо орг. лигандов, связанных с Мо через атом С, в молекулы обычно входят СО, фосфины, амины и др. Наиб. изучен бис[трикарбонил(циклопен тадиенил)молибден] пурпурно красные кристаллы, т. пл. 215 217°С (с разл.); раств.… … Химическая энциклопедия
Этилен — Этилен … Википедия
Источник
Фенилацетилен — Phenylacetylene
- 536-74-3
Y
- ChEMBL234833
Y
- 10364
Y
- 239WSR2IBO
Y
23,2 (водн., Экстраполировано)
 Y проверить ( что есть ?)
Y проверить ( что есть ?)  Y
Y  N
NФенилацетилен представляет собой алкиновый углеводород, содержащий фенильную группу. Он существует в виде бесцветной вязкой жидкости. В исследованиях иногда используется как аналог ацетилена ; будучи жидкостью, с ним легче обращаться, чем с газообразным ацетиленом.
СОДЕРЖАНИЕ
Подготовка
В лаборатории фенилацетилен может быть получен путем удаления бромистого водорода из дибромида стирола с использованием амида натрия в аммиаке :
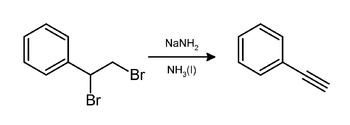
Его также можно получить путем удаления бромистого водорода из бромстирола с использованием расплавленного гидроксида калия .
Источник
ФЕНИЛАЦЕТИЛЕН
ФЕНИЛАЦЕТИЛЕН (этинилбензол), мол.м. 102,14; бесцв. жидкость; т. пл. — 44,8 0 C, т. кип. 141,7 0 C, 44 °С/18 мм рт. ст.; d 20 4 0,9281; n 20 D 1,5492; 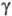
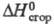
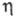
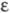
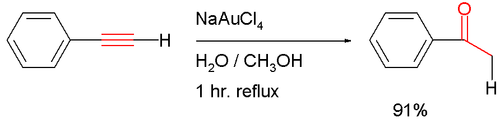
При гидратации разб. H 2 SO 4 фенилацетилен дает ацетофенон. Присоединяет Br 2 и I 2 с образованием соответствующих дигалогенстиролов; присоединение галогеноводородов приводит к 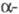
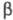
Ф енилацетилен легко полимеризуется, сополимеризуется с ацетиленом, метилметакрилатом, акрилонитрилом, стиролом, 2-винилпи-ридином и др. мономерами. При действии кислорода в присут. хлоридов Cu + или Cu 2+ в жидком пиридине димеризуется до дифенилбутадиина.
Ф енилацетилен получают нагреванием a- или b -галогенстиролов с C 2 H 5 ONa, KOH или Na в жидком NH 3 , кипячением a , b -дибромэтилбензолов с C 2 H 5 ONa, медленной перегонкой фенил-пропионовой к-ты с анилином (соотношение 1:4).
Ф енилацетилен- сшивающий агент, связующее в произ-ве нек-рых композиционных материалов. Раздражает слизистую оболочку дыхат. путей, кожу. ЛД 100 5 мл/кг (крысы, перорально).
Лит.: Kirk — Othmer encyclopedia, 3 ed., v. 1, N. Y., 1978, p. 192-193.
Источник
Acetyl
Это пилотный ролик из серии об органических реакциях.
Наведите курсор на ячейку элемента, чтобы получить его краткое описание.
Чтобы получить подробное описание элемента, кликните по его названию.
| H + | Li + | K + | Na + | NH4 + | Ba 2+ | Ca 2+ | Mg 2+ | Sr 2+ | Al 3+ | Cr 3+ | Fe 2+ | Fe 3+ | Ni 2+ | Co 2+ | Mn 2+ | Zn 2+ | Ag + | Hg 2+ | Pb 2+ | Sn 2+ | Cu 2+ | |
| OH — | Р | Р | Р | Р | Р | М | Н | М | Н | Н | Н | Н | Н | Н | Н | Н | — | — | Н | Н | Н | |
| F — | Р | М | Р | Р | Р | М | Н | Н | М | М | Н | Н | Н | Р | Р | Р | Р | Р | — | Н | Р | Р |
| Cl — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | Р | М | Р | Р |
| Br — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | М | М | Р | Р |
| I — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | Р | ? | Р | Р | Р | Р | Н | Н | Н | М | ? |
| S 2- | М | Р | Р | Р | Р | — | — | — | Н | — | — | Н | — | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| HS — | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | Н | ? | ? | ? | ? | ? | ? | ? |
| SO3 2- | Р | Р | Р | Р | Р | Н | Н | М | Н | ? | — | Н | ? | Н | Н | ? | М | М | — | Н | ? | ? |
| HSO3 — | Р | ? | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? |
| SO4 2- | Р | Р | Р | Р | Р | Н | М | Р | Н | Р | Р | Р | Р | Р | Р | Р | Р | М | — | Н | Р | Р |
| HSO4 — | Р | Р | Р | Р | Р | Р | Р | Р | — | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | Н | ? | ? |
| NO3 — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р |
| NO2 — | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | Р | М | ? | ? | М | ? | ? | ? | ? |
| PO4 3- | Р | Н | Р | Р | — | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| CO3 2- | Р | Р | Р | Р | Р | Н | Н | Н | Н | ? | ? | Н | ? | Н | Н | Н | Н | Н | ? | Н | ? | Н |
| CH3COO — | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р | Р | — | Р | Р | Р | Р | Р | Р | Р | — | Р |
| SiO3 2- | Н | Н | Р | Р | ? | Н | Н | Н | Н | ? | ? | Н | ? | ? | ? | Н | Н | ? | ? | Н | ? | ? |
| Растворимые (>1%) | Нерастворимые ( Спасибо! Ваша заявка отправлена, преподаватель свяжется с вами в ближайшее время. Вы можете также связаться с преподавателем напрямую: 8(906)72 3-11-5 2 Скопируйте эту ссылку, чтобы разместить результат запроса » » на другом сайте. Изображение вещества/реакции можно сохранить или скопировать, кликнув по нему правой кнопкой мыши. Если вы считаете, что результат запроса » » содержит ошибку, нажмите на кнопку «Отправить». Этим вы поможете сделать сайт лучше. К сожалению, регистрация на сайте пока недоступна. На сайте есть сноски двух типов: Подсказки — помогают вспомнить определения терминов или поясняют информацию, которая может быть сложна для начинающего. Дополнительная информация — такие сноски содержат примечания или уточнения, выходящие за рамки базовой школьной химии, нужны для углубленного изучения. Здесь вы можете выбрать параметры отображения органических соединений. Источник Adblockdetector |